首页 > 心得体会 > 学习材料 / 正文
化学链燃烧过程Fe2O3/Al2O3载氧体表面CH4反应:ReaxFF-MD模拟
2023-01-16 19:50:07 ℃袁妮妮,郭拓,白红存,何育荣,袁永宁,马晶晶,郭庆杰
(宁夏大学省部共建煤炭高效利用与绿色化工国家重点实验室,化学 化工学院,宁夏 银川 750021)
具有天然优势的Fe 基载氧体被广泛应用于CLC 示范和工业化装置。一般,通过加入惰性载体(例如:Al2O3,SiO2,MgO,ZrO,TiO2,MgAl2O4等)可有效增强Fe 基载氧体实际应用性[8-12],并促进其在CLC 过程中长周期稳定循环使用。文献中[13-15]报道了Fe 基载氧体中加入惰性载体对其宏观性能具有促进作用。例如,Bolt 等[16]和Abad 等[17]开展了关于Al2O3惰性载体负载Fe2O3载氧体(表示为:Fe2O3/Al2O3)CLC 过程中反应性的实验研究,结果表明:Al2O3惰性载体与Fe2O3相互作用生成了具有尖晶石结构FeAl2O4,FeAl2O4晶相的生成不仅促进了Fe2O3向Fe3O4的转化,而且促进了晶格氧的释放,并且显著提高了Fe2O3载氧体还原反应速率。此外,王保文等[13,18]对Fe2O3/Al2O3载氧体煤CLC 性能的研究,发现Al2O3惰性载体加入改变了Fe2O3载氧体颗粒形貌,对煤CLC 过程具有促进作用。至今关于CLC 过程Fe2O3/Al2O3载氧体颗粒在反应器内性能提升的微观机理和惰性载体的调控机制尚不清楚[16-17],这对负载型Fe基载氧体性能优化、工业应用和CLC 过程放大具有重要指导作用。目前相关机理研究仅限于Qin 等[19-20]采用量子化学方法在原子/分子尺度对Fe2O3载氧体表面添加单个惰性载体模型表面微观基元反应的研究,缺少颗粒-反应器尺度反应过程机理的深入和系统性探究。因此,本文将从原子/分子-颗粒-反应器尺度对Fe2O3/Al2O3载氧体表面CH4燃烧气-固反应过程、产物分布、反应机理和动力学特性等进行系统研究,并进一步探究Al2O3惰性载体负载机制和调控作用。研究将是Fe 基载氧体CLC工业示范装置和产业化的关键基础。
反应力场分子动力学(reactive force field molecular dynamics,ReaxFF-MD)方法可用于处理大体系多尺度气-固相复杂反应,并且该方法已广泛应用于复杂反应体系。例如,Zhu 等[21]成功地将ReaxFF-MD方法用于碳氢分子(C/H/O 元素构成的小分子)分别在金属Cu 和CuO 表面的催化转化和CLC 过程反应机理研究,计算精度与量子化学密度泛函理论计算相当,计算效率高,处理体系更大。此外,Li 等[22]关于不同燃料热解和燃烧反应ReaxFF-MD 模拟也证实了其应用的有效性。因此,ReaxFF-MD 方法可应用于化学链过程载氧体表面多相复杂反应过程模拟。至今关于CLC 过程惰性载体负载Fe 基载氧体表面CH4燃烧气-固反应过程及其气相产物生成机制的ReaxFF-MD 研究,文献中鲜有报道。CH4燃烧作为CLC 过程重要组成部分,关系CLC 过程放大效果和过程强化,对其进行研究具有重要的实际和工业应用价值。
本文拟借助ReaxFF-MD 方法[23-25],对CLC 过程中应用广泛的Fe2O3/Al2O3载氧体表面CH4反应过程模拟,考察温度对反应过程的影响;
探究反应过程中间体、自由基小分子及其产物分布随时间变化;
模拟CLC 过程反应器内载氧体颗粒表面CH4反应过程,一方面,从分子-颗粒尺度探究反应器内气体产物(CO2/CO/H2/H2O)的生成机制,进一步为反应器内气体产物种类的调控提供理论依据;
另一方面,探究CLC 过程Al2O3惰性载体对Fe2O3-CH4体系反应的调控机制,并采用ReaxFF-MD 方法,从分子-颗粒-反应器尺度探究CLC 过程Fe2O3/Al2O3载氧体表面CH4反应过程(表示为:Fe2O3/Al2O3-CH4)的调控机制,揭示Al2O3惰性载体负载对Fe2O3载氧体反应性调控的微观机制,为负载型Fe基载氧体产业化应用提供基础研究。
文中计算是采用阿姆斯特丹计算平台(Amsterdam modeling suite,AMS)中反应力场分子动力学ReaxFF 模块[26]完成。主要对CLC 过程反应器内Fe2O3/Al2O3-CH4体系反应过程ReaxFF-MD 模拟。计算中采用ReaxFF 模块自带C/H/O/Fe/Al/Ni/Cu/S/Cr/Si/Ge 力场参数[27-28],并采用NVT 正则系综分子动力学(NVT-MD)方法进行计算,步长为0.25 fs,模拟反应温度分别为1500、2000、2500、3000、3500 和4000 K,探究不同温度Fe2O3/Al2O3-CH4体系反应特性。计算模型由载氧体与CH4分子共同构成。反应前计算模型在298 K 进行了20000 步非反应(nonreaction)弛豫过程,使其处于基态。ReaxFF-MD 模拟过程累积1000000 步,总时长250 ps。计算中通过提高反应温度的方式有效增加分子有效碰撞次数,使反应尽量在较短时间内发生并完成[29]。通过反应温度的选择合理选取模拟计算所需时长,提高计算效率,该处理方法已在文献[25,30]中报道,具有计算结果与实验结果吻合较好的特征[31]。
文中选取α-Fe2O3(001)低指数晶面[32-35],并以Fe—O3—Fe…为反应表面的稳定结构为原胞,2×2扩胞得到超胞模型,如图1 所示。模型中间部分为Fe2O3/Al2O3载氧体,载氧体部分共包含15 层810 个原子,上下表面各4 层为Fe2O3活性组分构成的反应表面,中间7 层由Al2O3惰性载体构成。反应过程中Al2O3惰性载体中间3 层原子(蓝色标记部分)固定,剩余原子均弛豫,上下最表层均为CH4分子,该结构为驰豫后稳定结构,计算中选取30 Å× 30 Å× 60 Å(1 Å=0.1 nm)周期性盒子进行ReaxFF-MD 模拟。该模型更接近于实验中负载型Fe 基载氧体颗粒结构和惰性载体负载量(m(Al2O3)∶m(Fe2O3)= 40 ∶60),本文计算模型尚未见文献报道。

图1 Fe2O3/Al2O3载氧体与CH4反应模型Fig.1 The model of Fe2O3/Al2O3oxygen carrier reacted with CH4
ReaxFF-MD 计算中,通过势能(potential energy)计算体系能量和反应过程中能量变化趋势。势能由反应体系不同部分能量共同构成[31,36],具体如式(1)所示:

式中,势能Epotentialenergy分别由键能(Ebond)、过饱和键能(Eover)、不饱和键能(Eunder)、键角能(Eval)、共价键修正能(Epen)、二面角能(Etors)、共轭能(Econj)、范德华相互作用能(EvdWaals)和库仑作用能(Ecoloumb)共同构成。在ReaxFF模块势能计算中,各部分能量与键级(bond order)有关,而键级则是由键之间距离决定,如式(2)所示:
近日读绍兴文理学院人文学院教授邹志方先生所著《陆游研究》一书,其中竟有陆游 “初仕瑞安” 一节。文章从生平考察,作品考察,相关材料考察三个方面进行论述。文章多处以推理、猜想的方式,草率地下结论。在难以自圆其说的地方,则以 “应该承认是史实”“应作于”“肯定会”“似乎不大可能”来搪塞。例如 “曾幾的口许要两年半才实现,似乎不大可能”“二十六年冬出仕即官瑞安主簿的可能性,则相对大一些”①等等。拜读之余,惊诧不已。为此顺着邹先生的三方面,就陆游有否“初仕瑞安”与邹先生商榷。

2.1 模拟温度
分别考察了温度为1500、2000、2500、3000、3500和4000 K 时,CLC 过程Fe2O3/Al2O3-CH4体系反应过程ReaxFF-MD 模拟。首先,探究了反应温度对体系势能的影响,如图2(a)所示。由图可知,不同反应温度Fe2O3/Al2O3-CH4体系势能曲线不同。当反应开始后,随着中间体、自由基小分子和产物的生成,体系势能逐渐降低,并且反应温度越高体系势能降低越明显,表明反应过程为放热,高温有利于Fe2O3/Al2O3载氧体表面CH4氧化。其中,反应温度为3000 K时,随着反应进行体系势能曲线逐渐降低,在200~250 ps时,势能降至最低并基本保持稳定,为最低势能曲线,表明CH4氧化体系达到反应平衡,CH4分子数目降至最低并且基本稳定,如图2(b)所示。因此,3000 K 是CH4在Fe2O3/Al2O3载氧体表面氧化放热的较优温度。

图2 化学链燃烧过程CH4在Fe2O3/Al2O3载氧体表面不同温度氧化势能曲线(a)和CH4分子数目变化趋势(b)(1 kcal=4.18 kJ)Fig.2 Potential energy curves(a)and the number of CH4molecules(b)of the oxidation of CH4 on the surface of Fe2O3/Al2O3 oxygen carriersin chemical looping combustion at various temperature
此外,考察了反应过程中不同温度下CH4分子数目变化趋势,如图2(b)所示。由图可知,不同反应温度下CH4分子不断被氧化减少,变化趋势与反应过程体系势能变化一致。当反应温度大于等于3000 K 时,反应体系逐渐达到平衡,CH4分子数目降至最低甚至为零。以上研究表明:CH4在Fe2O3/Al2O3载氧体表面的氧化过程为放热反应,3000 K 时放热量最大,为较优反应温度。
2.2 CH4氧化过程及其产物分布
图3 是Fe2O3/Al2O3-CH4和Fe2O3-CH4体系化学链燃烧过程模拟结果,包括生成中间体和产物的时间及生成量曲线,曲线斜率代表生成速率。该过程中Fe2O3/Al2O3和Fe2O3载氧体主要提供CH4氧化所需晶格氧,Al2O3惰性载体对氧化过程具有显著调控作用。由图3(a)可知,在3000 K 较优反应温度,Fe2O3/Al2O3-CH4体系反应过程、中间体、产物及其反应速率等如下所示:

图3 3000 K化学链燃烧过程CH4分子在载氧体表面反应过程产物分布及其分子数目Fig.3 Production distribution and their molecule number of the reaction process of CH4 on thesurface of oxygen carriers during chemical looping combustion at 3000 K

随着CH4分子不断被氧化分子数目逐渐减少。首先,主要发生式(3)反应生成产物H2O,整个反应过程随着反应进行,H2O 分子逐渐增加;
175 ps 时,式(3)反应达到平衡,H2O 分子数目达到最大并保持稳定。式(4)反应产物为H2,H2分子数目明显低于H2O分子数目。反应进行到15 ps时,式(5)反应开始生成产物CO。反应分别进行到40 ps和75 ps时,式(6)和式(7)反应分别开始生成产物CO2和C。反应进行到190 ps 时,CO2和C 产物均消失,CO 产物分子数目略微增大,表明CO2和C 再反应生成CO 产物,发生式(8)反应,有利于合成气CO和H2生成。
根据上述反应过程,燃料反应器中CH4在Fe2O3/Al2O3载氧体表面氧化反应及其反应速率如图4所示。

图4 化学链燃烧过程CH4在Fe2O3/Al2O3载氧体表面反应过程及产物示意图Fig.4 Schematic of the reaction process and production distribution of CH4 on the surface of Fe2O3/Al2O3 oxygen carrier during chemical looping combustion
Fe2O3/Al2O3载氧体表面CH4氧化过程,反应从式(3)到式(8)顺序依次进行,反应速率如下:

式(6)和式(7)反应生成产物CO2和C,然后CO2和C 发生式(8)反应生成CO,体系中CO 分子数目略微增加。
如图3(b)所示,CLC 过程燃料反应器内Fe2O3载氧体表面CH4氧化反应、产物分布和反应速率等如下所示:
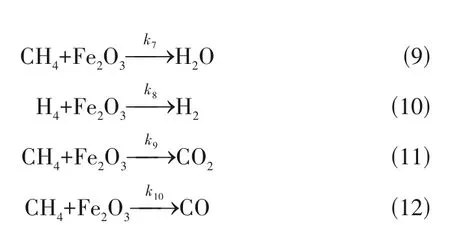
由图3(b)可知,CH4在Fe2O3载氧体表面氧化反应过程中,随着CH4分子不断氧化减少,首先,主要发生式(9)反应生成产物H2O,并且整个反应过程中,生成H2O分子数目最多。式(10)反应生成产物H2,H2分子数目明显低于H2O,k7远大于k8。反应进行到10 ps 时,式(11)反应开始生成产物CO2,该反应很快达到平衡。反应进行到20 ps 时,式(12)反应开始发生,生成产物CO。随着反应进行CH4分子数目进一步减少,CO生成速率出现先增大后稳定的趋势。
Fe2O3表面CH4氧化燃烧过程如图5 所示,反应从式(9)到式(12)顺序依次进行,且反应速率关系为:k7>k8>k10>k9。该过程不同于Fe2O3/Al2O3表面CH4氧化过程,反应速率明显降低。Fe2O3表面反应产物中包含了CO2,而Fe2O3/Al2O3表面生成的CO2与C 再反应完全转化为CO,表明Fe2O3/Al2O3表面CH4氧化过程有利于合成气(CO和H2)的生成。

图5 化学链燃烧过程CH4在Fe2O3载氧体表面氧化过程及产物示意图Fig.5 Schematic of the oxidation process and production distribution of CH4 on the surface of Fe2O3oxygen carrier during chemical looping combustion
由Al2O3惰性载体负载前后Fe2O3载氧体表面CH4氧化过程模拟可知:Al2O3惰性载体加入影响CH4在Fe2O3载氧体表面的氧化过程,主要表现为反应体系势能、产物种类、反应过程和中间体等不同,并且生成相同产物速率不同。反应过程特征如下。
(1)反应过程体系势能不同。3000 K 较优反应温度时,Fe2O3/Al2O3载氧体表面CH4氧化反应过程体系势能明显低于Fe2O3载氧体表面,表明Fe2O3/Al2O3载氧体表面CH4氧化过程放出更多热量。
(2)反应过程、中间产物及其速率不同。3000 K时,Fe2O3/Al2O3载氧体表面CH4氧化过程,生成产物H2O的速率明显高于Fe2O3载氧体表面反应,即k1>k7,生成产物H2O分子数目明显多于Fe2O3载氧体表面氧化过程。而H2的生成则是Fe2O3载氧体表面过程速率较高,即k2<k8。此外,Fe2O3/Al2O3载氧体表面CH4氧化过程,产物CO2和C 再反应转化为CO[式(8)],该过程有利于合成气产物CO 和H2生成。而Fe2O3载氧体表面反应生成产物CO2和CO,相同产物生成量不同。

2.3 Al2O3惰性载体作用机制
为了探究Al2O3惰性载体对Fe2O3-CH4体系反应过程的作用机制,首先考察了Al2O3惰性载体对体系反应过程晶格氧释放量的影响,释氧量越大,越有利于CH4氧化。晶格氧释放量X计算过程如式(13)所示:

式中,Q0和Q1分别表示反应开始和结束时载氧体中晶格氧数目。通过式(13)计算得到Fe2O3-CH4和Fe2O3/Al2O3-CH4体系晶格氧释放量分别为32.1%和35.7%,表明Al2O3惰性载体存在增大了Fe2O3载氧体中晶格氧的释放量。
在3000 K 较优反应温度下,探究Al2O3惰性载体加入对Fe2O3-CH4体系氧化过程势能的影响,如图6 所示。由图可知,Fe2O3-CH4体系初始势能最低;
10~250 ps之间,体系反应达到平衡,势能基本保持稳定,体系热量不再变化。然而,Fe2O3/Al2O3-CH4体系整个氧化过程中势能逐渐降低,并且势能明显低于Fe2O3-CH4体系氧化过程,放热效果显著,表明Al2O3惰性载体负载Fe2O3载氧体表面更有利于CH4氧化放热,促进CO 和H2合成气产物生成。该结果与王保文等[13]和Hu 等[37]关于Fe2O3/Al2O3载氧体分别用于煤CLC 和水稻秸秆化学链气化过程反应性增强实验结果一致。CLC/气化过程中,Fe2O3载氧体反应性增强主要是Al2O3惰性载体加入使Fe2O3载氧体颗粒表面积和孔径等微观形貌结构优化的结果。本文ReaxFF-MD 计算表明:Al2O3惰性载体增强了CLC过程中Fe2O3表面CH4氧化,主要是Al2O3惰性载体与Fe2O3活性组分相互作用,对Fe2O3载氧体颗粒中晶格氧具有活化作用,促进了Fe2O3活性相中晶格氧的迁移-扩散-释放,从而明显提高了载氧体中晶格氧的释放速率和释放量,有利于CLC 过程CH4氧化转化,作用机制如图7 所示。此外,冯于川[38]关于ZrO 和MgAl2O4惰性载体负载NiO 载氧体表面CH4和CO 反应量子化学研究,也证实了惰性载体加入对NiO 活性相也具有活化作用,主要是降低了表面反应活化能。

图6 3000 K时CH4分别在Fe2O3和Fe2O3/Al2O3载氧体表面氧化反应势能曲线Fig.6 Potential energy curves of the reaction process of CH4 on the surface of Fe2O3and Fe2O3/Al2O3oxygen carrier at 3000 K,respectively

图7 化学链燃烧过程Fe2O3/Al2O3-CH4体系(a)和Fe2O3-CH4体系(b)作用机制示意图Fig.7 Schematic of the interaction mechanism of Fe2O3/Al2O3-CH4 system(a)and Fe2O3-CH4 system(b)during chemical looping combustion process
本文应用ReaxFF-MD 方法对CLC 过程Fe2O3/Al2O3载氧体表面CH4反应过程及其中间体、产物种类、反应过程热量变化等进行模拟,探究了Al2O3惰性载体加入对反应过程的调控机制,主要结论如下。
(1)不同温度下,Fe2O3和Fe2O3/Al2O3载氧体表面CH4氧化均为放热过程,反应过程势能均降低,并且Fe2O3/Al2O3载氧体表面CH4氧化过程势能降低更明显,放出热量更多。Al2O3惰性载体加入增大CLC 过程Fe2O3-CH4体系反应过程热量输出。
(2)Al2O3惰性载体对Fe2O3-CH4氧化过程具有显著增强作用。Al2O3对Fe2O3载氧体活性相颗粒中晶格氧的活化作用,促进了晶格氧的迁移-扩散-释放,增大了Fe2O3载氧体中晶格氧的释放速率和释放量,促进CH4氧化。
(3)Al2O3惰性载体添加改变了化学链燃烧过程Fe2O3载氧体反应性和Fe2O3/Al2O3-CH4体系反应的热力学和动力学行为。主要是促进了Fe2O3载氧体表面CH4氧化,并对CH4反应过程、中间体、产物及其反应速率和放热量等均具有显著促进和调控作用,促进了含C物质向合成气的转化应用,减少了温室气体排放,实现能源高效转化及碳减排目标。
猜你喜欢 势能惰性产物 惰性知识爱你·健康读本(2019年7期)2019-11-22惰性知识爱你(2019年25期)2019-07-16时代的流行产物小雪花·初中高分作文(2017年10期)2018-05-15势能的正负取值及零势能面选择问题初探高中生学习·高三版(2017年9期)2017-10-26美联储加息的产物研究今日财富(2017年32期)2017-10-19“动能和势能”“机械能及其转化”练习中学生数理化·八年级物理人教版(2016年5期)2016-08-26弹性势能纵横谈新高考·高一物理(2015年3期)2015-08-20关于重力势能和弹性势能理解与运用的几个典型错误新高考·高一物理(2014年4期)2014-09-17惰性,人性中最可怕的敌人农业知识·百姓新生活(2014年3期)2014-04-25化学问答中学生数理化·高二版(2008年5期)2008-11-12猜你喜欢
- 2024-01-20 有关于第五次全国经济普查统计重点业务综合培训大会上讲话(完整文档)
- 2024-01-20 “严纪律、转作风、保安全、树形象”专题学习教育活动通知(完整文档)
- 2024-01-20 2024XX区住房城乡建设工作情况汇报
- 2024-01-20 2024高校思政教育交流材料:善用反腐败斗争这堂“大思政课”(精选文档)
- 2024-01-20 2024年主题教育专题党课辅导报告,(4)
- 2024-01-20 关于赴某地学习考察地方立法工作情况报告(范文推荐)
- 2024-01-20 2024年度关于增强党建带团建工作实效对策与建议(精选文档)
- 2024-01-20 教师演讲稿:春风化雨育桃李,,潜心耕耘满芬芳(全文)
- 2024-01-20 主题教育第二阶段来了
- 2024-01-20 2024年度关于到信访局实践锻炼个人总结【完整版】
- 搜索
-
- 打赌输了任人处理作文1000字7篇 05-12
- 当代大学生在全面建设社会主义现代化强 05-12
- 全面建成社会主义现代化强国的战略安排 03-10
- 个人廉洁自律方面存在的问题及整改措施 05-12
- 谈谈青年大学生在中国式现代化征程上的 05-12
- 2022年党支部第一议题会议记录(全文完 11-02
- 作为青年大学生如何肩负时代责任6篇 05-12
- 村党组织建设现状及工作亮点存在问题与 05-12
- 全面从严治党,自我革命重要论述研讨会 05-12
- 产业工人队伍建设改革(全文完整) 10-31
- 11-25国庆70周年庆典晚会 庆典晚会串词
- 11-25办公室礼仪的十大原则 浅谈办公室的电话礼仪
- 01-17用心灵轻轻地歌唱_心灵的歌唱
- 01-17也许你不是我一生的唯一|也许不是我
- 01-17爱了,请珍惜;不爱,趁早放手|爱就珍惜不爱就放手
- 01-17岁月带走的是记忆,但回忆会越来越清晰|有趣又有深意的句子
- 01-17曾经的美好只是曾经,我只想珍惜身边的人|我只想珍惜你
- 01-18从容不惊 [学会笑眼去看世界,不惊不乍,淡定从容]
- 02-03当代大学生学习态度调查报告
- 02-03常用护患英语会话
- 标签列表
